“Miastenia Gravis: un iceberg a la deriva”
Vivir con MIASTENIA GRAVIS AUTOINMUNE (enfermedad neuromuscular crónica y rara) es complicado. No todos la padecemos por igual, su impacto va a depender de diferentes condicionantes, tanto de la propia enfermedad como de la peculiaridad del paciente…y por supuesto, del profesional que “nos toque”. Por tanto, hay que tener suerte con este pool de circunstancias porque van a influir sin duda en nuestra calidad de vida
En un día como hoy, día de su visibilidad mundial, y al igual que otros años, me gusta resaltar al protagonista, que por su puesto no es la enfermedad, aunque la mayoría de los titulares de Asociaciones, Sociedades y Medios de Comunicación se empeñen en las típicas cifras sobre el números de afectados y de diagnosticados cada año en nuestro país, o esas otras afirmaciones concluyendo que la mayoría de los pacientes podemos hacer una “vida normal”, o si ya disponemos de nuevos tratamientos, etc, etc y etc… porque cada año y en esta fecha, parece ser lo que llama la atención, y aunque dejan números y comentarios interesantes e impactantes, solo sigue siendo la “punta del iceberg”. Padecer y sobrellevar esta enfermedad, por su complejidad, es como un iceberg a la deriva, si no controlas la situación podría representar un grave problema…porque lo grande (bummock) se encuentra oculto y es poco conocido

Comentaba, que había que tener “suerte” con las circunstancias cuando toca sobrellevar una enfermedad de estas características (más adelante pondré algunas). Respecto a la propia Miastenia no da igual debutar con problemas deglutorios (disfagia) o respiratorios que hacerlo solamente con una caída del párpado (ptosis), ni tener anticuerpos ACRA en vez de anti-MUSK, ni presentar una hiperplasia de la glándula del timo en vez de un timoma (tumor), ni que aparezca antes de los 50 años que hacerlo después. Tampoco, tener o no ciertos factores de riesgo como padecer otra enfermedad autoinmune conjuntamente (o varias), llevar una vida sedentaria, ser fumador o vivir en un continuo estrés. Y como que no es lo mismo estar en manos de un buen profesional (o Equipo de Salud) que más o menos esté actualizado y sepa por donde “van los tiros” cuando el diagnostico parece no estar claro, hay una mala evolución clínica, o persiste la falta de respuesta a los tratamientos, y ya puestos a pedir, que pueda conocer el impacto personal al que te enfrentas (que ya sería para nota)…Pues si, asi es, que estas circunstancias te favorezcan es tener suerte, bastante suerte, porque muchos de nosotros hemos caído en el “lado bueno” de la Miastenia (por decir algo, aunque no quita haberlo pasado mal sobre todo por no saber a qué te enfrentabas), por tener un diagnostico más o menos precoz, disponer de un tratamiento efectivo, optar a un profesional actualizado y por lograr el gran objetivo de conseguir la REMISION de la enfermedad (total o farmacológica)…esto es ser un «paciente miastenico afortunado”. Y sería como estar también en la punta del iceberg, se nos ve bien, parecemos estables, podemos trabajar, y hasta ir al gym y divertirnos…Pero esto no debe solapar la otra realidad, la cruda, la que tiene la gran mayoría de los afectados, esos que han caído al otro lado y que no pueden dejar su agresiva medicación, esos de las continuas recaídas, y crisis, y hospitalizaciones en UCI (un 7-8% por desgracia fallecen), y depresiones, y despidos laborales, y fracasos matrimoniales…si, esos, para mí son los auténticos héroes y heroínas que habría que ensalzar en un día tan señalado, no solo por como te impacta la enfermedad a todos los niveles (las enfermedades crónicas son así) sino por como la Miastenia te controla, maneja y juega contigo, como te permite que estés libre de síntomas unas horas o quizá unos días para luego volver a hundirte, y así una vez y otra y otra y otra…¿cómo se aguanta esto? ¿como puedes adaptarte a esa ambivalencia? ¿qué fuerza mental hay que mantener para afrontar este juego cotidiano donde tu eres la marioneta y la Miastenia la mano que mueve los hilos?…a ellos son a los que hay que «visibilizar» un 2-junio
Y sobre esto se habla poco en este día, quizá no pegue mucho una reflexión tan profunda y personal, y tal vez con los titulares de siempre sea suficiente…bueno, sea como fuere, ayuda para saber que la Miastenia Gravis también existe
Para la sociedad esta realidad del paciente es muy poco conocida. Somos muy vulnerables porque nuestras capacidades están alteradas y muy limitadas, y demasiadas veces la invisibilidad de los síntomas juega en nuestra contra (a no ser que te vean con un parche en el ojo, en una silla de ruedas o con una sonda de alimentación sujeta a la nariz), y en este día, DÍA MUNDIAL DE LA MIASTENIA, se suele pasar de puntillas sobre ello, creo que habría que ir cambiando la perspectiva y la tendencia e incidir más en la problemática individual, igualar más las intervenciones entre las entrevistas médicas (lo más frecuente y al parecer lo más significativo) con los testimonios del paciente (mucho más escasos) que para mí siempre seguirán siendo lo más relevante un 2 de junio. Es lo que tiene el iceberg, que para ver su dimensión hay que sumergirse y contemplarlo


Son ya muchos años formando parte de este “ICEBERG MIASTÉNICO”. Personalizando diré que entre 2003-2007 me toco estar bastante jodido y hundido en ese lado oscuro al que pertenece la gran mayoría, por suerte, desde el 2008 ocupo el otro lugar, ese que sobresale brillante y resplandeciente, y con el que sueñan muchos: el de la Remisión Total (sin síntomas importantes y sin necesidad de medicación). Estar en el lado oscuro me hizo reflexionar y aprender, sentir lo vulnerable que eres y qué cerca tienes las dificultades, percibir el miedo ante la incertidumbre, cómo cambia tu ánimo tan rápido, la incomprensión que te suele rodear, pero sobre todo, me hizo entender la necesidad que tenemos de ayuda para reconducir nuestra vida ante el cambio tan brutal que hemos tenido. Y esta sigue siendo mi motivación, actuar y colaborar para que muchos más intenten alcanzar la Remisión de la enfermedad, porque ello conlleva mejorar, y mucho, tu calidad de vida…lo merecemos!!
Y por ello administro «MIASTENIA GRAVIS ANDALUCÍA» (en Facebook), un Grupo de Autoayuda internacional, con más de 3.000 miembros hispanohablantes afectados de Miastenia Gravis (y familias) que buscan mejorar su vida mediante la INFORMACIÓN y EDUCACIÓN en la enfermedad, a través de una CONSULTA ENFERMERA PERMANENTE basada en la evidencia científica y profesional de nuestra fuente www.miasteniaysalud.com Esta Consulta obedece a la demanda continua de los pacientes por encontrar “respuestas rápidas” a sus problemas con la Miastenia, unas respuestas fundamentadas en el estudio actualizado y en mi experiencia como paciente (22 años) donde voy aportando mis RECOMENDACIONES que ayuden en las actividades del día a día así como orientar sus próximas revisiones médicas. No olvidemos que en muchos países no funciona el Sistema de Salud como se desearía, con escasos recursos y  pobre acceso a los tratamientos, ni tampoco ignorar como en muchos Hospitales de nuestro país las Consultas médicas siguen masificadas, con un tiempo de atención corto y Revisiones con mucha demora. Estas circunstancias, y tratándose la Miastenia de una patología rara, discapacitante, donde la sintomatología fluctúa con excesiva frecuencia hacen en la actualidad que un Grupo de Autoayuda de Enfermería en una Red Social sea una herramienta valiosa, muy útil y de gran relevancia para el paciente y su familia
pobre acceso a los tratamientos, ni tampoco ignorar como en muchos Hospitales de nuestro país las Consultas médicas siguen masificadas, con un tiempo de atención corto y Revisiones con mucha demora. Estas circunstancias, y tratándose la Miastenia de una patología rara, discapacitante, donde la sintomatología fluctúa con excesiva frecuencia hacen en la actualidad que un Grupo de Autoayuda de Enfermería en una Red Social sea una herramienta valiosa, muy útil y de gran relevancia para el paciente y su familia
Fdo: ANTONIO BARRANCO. Enfermero/Paciente de Miastenia Gravis
Miastenia Gravis Autoinmune
-
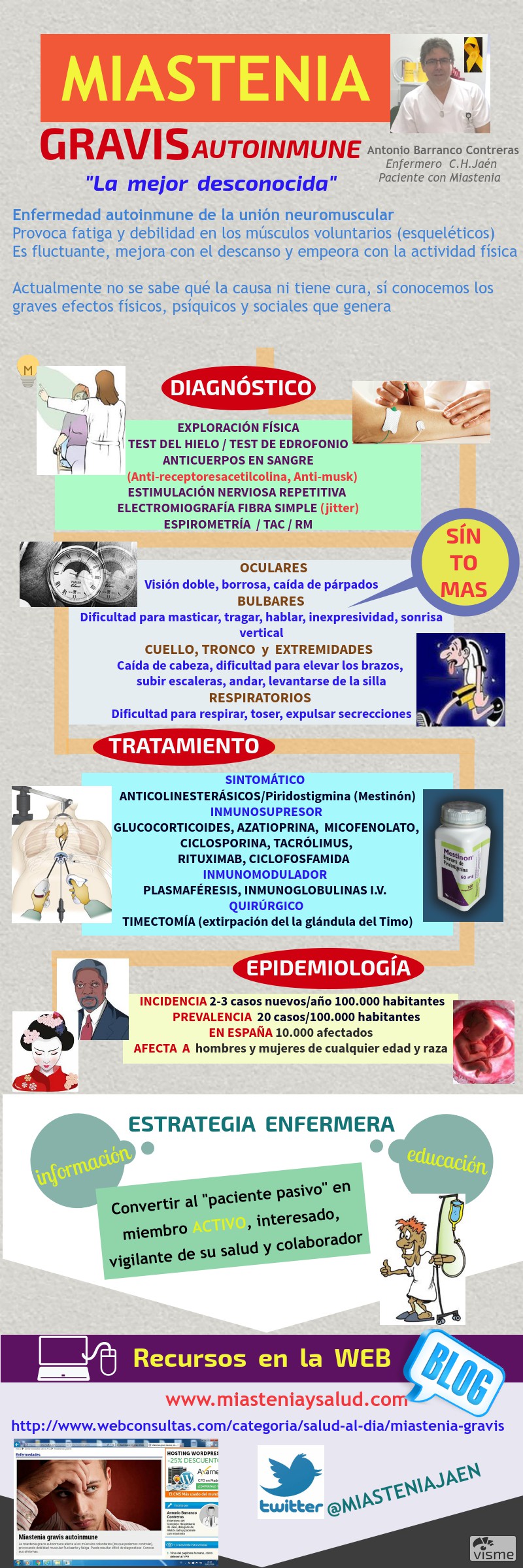
- Enfermedad neuromuscular, autoinmune, crónica y catalogada como rara
- Afecta a la unión del nervio con el músculo (exclusivamente a músculos voluntarios) causando debilidad y fatiga muscular fluctuante, mejora con el descanso y empeora con la actividad física sobre todo si es intensa y mantenida
- Puede aparecer en cualquier edad (mayor incidencia en mujeres 20-40 años y hombres 60-70)
- Sus principales síntomas son:
- visión doble
- caída de párpados
- dificultad para hablar, masticar, tragar, mantener erguida la cabeza
- incapacidad para levantar los brazos y caminar
- dificultad respiratoria (en su fase más severa)
-
- Actualmente no tiene cura, genera diferentes grados de discapacidad así como importantes problemas psicológicos, sociales y laborales
- El diagnóstico precoz, un tratamiento inmunosupresor eficaz y la educación del Paciente/Familia son claves para sobrellevarla y mejorar la calidad de vida
Según la Sociedad Española Neurología (SEN)
(Datos 2024)
√ Hay 15.000 personas afectadas de Miastenia Gravis Autoinmune en España
√ Cada año se diagnostican en España unos 700 nuevos casos. El 60% de ellos durante el primer año de experimentar los primeros síntomas, aunque puede existir un retraso en el diagnóstico de hasta 3 años
√ Mujeres menores de 40 años y hombres mayores de 60 son los grupos de edad más afectados. Entre un 10-20% la miastenia debuta en edad infanto-juvenil
√ En un 10-15% de los pacientes la enfermedad es grave y presenta mayor riesgo de mortalidad
√ El 70% de los pacientes nunca podrá dejar la medicación, y el 9% son farmacorresistentes (Miastenia Refractaria) sin mejoría y con frecuentes recaídas
 Soy ANTONIO BARRANCO. Paciente de Miastenia Gravis. Enfermero del Hospital Clínico Virgen de la Victoria (Málaga). En mi tiempo libre me dedico, sin ánimo de lucro, a EDUCAR en la enfermedad a los pacientes/familias de nuestro país y habla hispana, para ello utilizo varias herramientas:
Soy ANTONIO BARRANCO. Paciente de Miastenia Gravis. Enfermero del Hospital Clínico Virgen de la Victoria (Málaga). En mi tiempo libre me dedico, sin ánimo de lucro, a EDUCAR en la enfermedad a los pacientes/familias de nuestro país y habla hispana, para ello utilizo varias herramientas:
-
- Consulta Telefónica: 639 313 405
- Mail: antoniobc62@gmail.com
- Web: www.miasteniaysalud.com (única Web de nuestro país dedicada a la atención integral del paciente con Miastenia Gravis)
- En Facebook: Grupo de Autoayuda “MIASTENIA GRAVIS ANDALUCÍA” Consulta Enfermera de Miastenia permanente
- En Twitter: @MIASTENIAJAEN





 Soy ANTONIO BARRANCO, paciente de Miastenia Gravis con 20 años de experiencia, enfermero del Hospital Clínico Virgen de la Victoria (Málaga) y en mi tiempo libre me dedico a EDUCAR (sin ánimo de lucro) a los pacientes/familias de todos los puntos de nuestro país, y para ello utilizo varias herramientas:
Soy ANTONIO BARRANCO, paciente de Miastenia Gravis con 20 años de experiencia, enfermero del Hospital Clínico Virgen de la Victoria (Málaga) y en mi tiempo libre me dedico a EDUCAR (sin ánimo de lucro) a los pacientes/familias de todos los puntos de nuestro país, y para ello utilizo varias herramientas:























 Dicho esto, hay pacientes que prefieren vivir con un control aceptable de la Miastenia (aunque no el ideal) y haciendo adaptaciones en su vida que tener que enfrentarse a la incertidumbre de un cambio en su medicación…aunque esto tiene también otra lectura, y es que el miedo a empeorar las cosas por cambiar de tratamiento (que surja una exacerbación o crisis) puede conducir a llevar una vida con los síntomas mal controlados…que también puede ser peligroso
Dicho esto, hay pacientes que prefieren vivir con un control aceptable de la Miastenia (aunque no el ideal) y haciendo adaptaciones en su vida que tener que enfrentarse a la incertidumbre de un cambio en su medicación…aunque esto tiene también otra lectura, y es que el miedo a empeorar las cosas por cambiar de tratamiento (que surja una exacerbación o crisis) puede conducir a llevar una vida con los síntomas mal controlados…que también puede ser peligroso